Тепло и электропроводность цинка
В таблице представлена температурная зависимость теплофизических параметров цинка Zn таковых, как плотность цинка, теплоемкость, температуропроводность, теплопроводимость и его удельное электронное сопротивление. Теплофизические характеристики цинка указаны при температуре от 50 до 1000 К (-223 до 727°С).
Цинк при обычных критериях достаточно хрупкий и мерклый сплав, который плавится при температуре 692,7 К (около 420°С). При комнатной температуре плотность цинка равна 7130 кг/м 3 , что меньше плотности стали, но существенно больше (в 2,64 раза) плотности алюминия.
Плотность цинка при увеличении его температуры понижается, так как происходит повышение удельного размера этого сплава (цинк расширяется). К примеру, при температуре 1000 К цинк находится уже в водянистом состоянии, и плотность цинка становится равной 6570 кг/м 3 .
Характеристики цинка в водянистом состоянии претерпевают значимые конфигурации. Из таблицы отлично видно, что плотность водянистого цинка имеет наименьшее значение, чем плотность твердого сплава.
Также значительно понижаются значения таковых параметров цинка, как температуропроводность и теплопроводимость. Температуропроводность цинка в жестком состоянии убывает с увеличением температуры и увеличивается — в водянистом. Теплопроводимость цинка в жестком состоянии имеет отрицательный температурный коэффициент и положительный — в водянистом, она носит электрический нрав. При комнатной температуре теплопроводимость цинка равна 115 Вт/(м·град), что сравнимо с теплопроводимостью дюралевых сплавов.
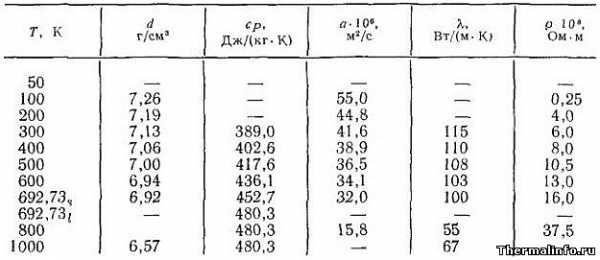
Зависимость удельной теплоемкости цинка от температуры является обычной для обычных металлов. Выше температуры Дебая теплоемкость слабо зависит от значения температуры. Дебаевская температура цинка близка к комнатной температуре. Теплоемкость цинка при его плавлении возрастает с 453 до 480,3 Дж/(кг·град)
Удельное электронное сопротивление цинка при переходе его в жидкое состояние существенно возрастает. По сопоставлению с иными сплавами, цинк различается умопомрачительно малой анизотропией удельного электронного сопротивления при температуре выше 100 К. В целом, температурная зависимость удельного электросопротивления цинка близка к линейной, хотя и наблюдается некий рост температурного коэффициента с увеличением температуры.
Источник:
В. Е. Зиновьев. Теплофизические характеристики металлов при больших температурах.
Коэффициент теплопроводимости металлов (Таблица)
Теплопроводимость почти всех металлов следует соотношению k = 2,5·10 -8 σT, где Т обозначает температуру в °К, а σ — электропроводность в единицах (ом·см) -1 . Это соотношение, которое идеальнее всего оправдывается для добротных проводников электро энергии и при больших температурах, можно использовать и для определения коэффициентов теплопроводности.
Соотношение kpcp=const, где р обозначает плотность, а ср — удельную теплоемкость при неизменном давлении, было предложено Стормом для того, чтоб разъяснить температурные конфигурации этих величин для неких металлов и сплавов.
Таблица коэффициент теплопроводимости металлов
Элементы с железной электропроводностью (числа, набранные курсивом, относятся к водянистой фазе)
Коэффициент теплопроводимости металлов при температура, °С
Таблица коэффициент теплопроводимости полупроводники и изоляторы
Коэффициент теплопроводимости при температура, °С
Теплопроводимость полупроводников
Представлена таблица теплопроводимости полупроводников при низкой отрицательной и положительной температурах — в интервале от -263 до 27°С.
Процесс теплопереноса в жестком теле в общем случае протекает за счет движения вольных носителей заряда и колебаний сетки атомов. Соответственно, выделяют две составляющие теплопроводимости: решеточную и электрическую. Общая теплопроводимость материала определяется суммой этих величин.
В сплавах количество вольных электронов довольно велико, и электрическая составляющая теплопроводимости заносит главный вклад в общую теплопроводимость — движение вольных заряженных частиц является главным механизмом переноса тепла в сплавах. Электрическая составляющая определяется сначала удельным электронным сопротивлением металлов и их температурой — чем эти характеристики меньше, тем выше теплопроводимость большинства металлов.
Диэлектрикам характерна сеточная (либо фононная) теплопроводимость, при которой процесс переноса тепла происходит за счет передачи энергии термических колебаний примыкающих атомов сетки. Электрическая составляющая переноса тепла в диэлектриках фактически отсутствует из-за малого количества вольных носителей заряда.
Теплопроводимость полупроводников обычно обоснована решеточной составляющей теплопроводимости. Но, некие полупроводники с высочайшим содержанием легированных добавок, содержат огромное количество вольных электронов (либо дырок) и имеют высочайший уровень электрической теплопроводимости и низкую фононную проводимость. К таковым полупроводникам можно отнести, к примеру, теллурид свинца PbTe и висмута Bi2Te3.
Температурная зависимость коэффициента теплопроводимости полупроводников определяется в главном их хим составом и степенью легирования. Теплопроводимость таковых полупроводников, как ZnSb, CdS, CdSe, CdTe и остальных миниатюризируется при повышении температуры. Но, воздействие температуры на теплопроводимость неких полупроводников таково, что при ее увеличении она поначалу возрастает, а потом начинает понижаться. К таковым полупроводникам можно отнести: GaP, AlN, AlSb и некие остальные.
Теплопроводимость полупроводников при комнатной температуре находится в широком спектре. По данным таблицы видно, что при температуре 27°С ее величина имеет значение от 1,7 (у HgSe n-типа) до 490 Вт/(м·град) у SiC n-типа. Любопытно отметить, что коэффициент теплопроводимости полупроводника SiC n-типа имеет величину огромную, чем теплопроводимость меди и серебра при данной же температуре.
Теплопроводимость полупроводников при разных температурах, Вт/(м·град)| t, °С → | -263 | -253 | -233 | -193 | -123 | 27 |
|---|---|---|---|---|---|---|
| Cd3As2 нелегированный, n=2·10 18 см -3 | — | — | — | — | 2,7 | 2,8 |
| CdSb p-типа, n=(3…5)·10 15 см -3 | — | — | — | 4,9 (-173°С) | 3,0 | 1,9 |
| ZnSb, чистота начального материала 99,9999% | 260 | 210 | 40 | 11,5 | 5,2 | 5,0 |
| ZnO *1 , концентрация примесей наименее 2,5·10 18 см -3 | 300 | 520 | 450 | 260 | 134 | 54 |
| ZnS, гексагональная структура, концентрация примесей наименее 5·10 17 см -3 | 300 | 380 | 310 | 155 | 70 | 27 |
| CdS, концентрация примесей наиболее 10 16 см -3 , || оси c | 540 | 360 | 200 | 97 | 43 | 20 |
| CdSe n-типа, чистота начального материала наиболее 99,99%, нелегированный, || оси c | 230 | 200 | 72 | 32 | — | — |
| CdTe, концентрация примесей наименее 2·10 18 см -3 | 520 | 250 | 117 | 44 | 18,4 | 7,5 |
| HgSe n-типа, n(при 4,2 К)=2,1·10 17 см -3 | 120 | 93 | 41 | 11 | 4,4 | 1,7 |
| HgTe p-типа, концентрация акцепторов 10 18 …10 19 см -3 | — | — | 25 (-213°С) | 14 | 5,0 | 2,6 |
| BN *2 | — | 2,0 | 10 | 43 | 112 | 180 |
| GaP p-типа, R(при 27°С)=75 см 3 /Кл | 190 | 590 | 700 | 450 | 210 | 140 (-23°С) |
| GaAs n-типа, n(при -196°С)=2·10 16 см -3 | 1400 | 2500 | 780 | 270 | 105 | 58 |
| GaSb p-типа, n=1,5·10 17 см -3 | 140 | 340 | 320 | 180 | 85 | 36 |
| InP n-типа, n(при -196°С)=2·10 16 см -3 | 1800 | 2700 | 1200 | 470 | 190 | 70 |
| InAs n-типа, n(при -196°С)=3·10 16 см -3 | 2900 | 1700 | 600 | 170 | — | — |
| InSb n-типа, n=7·10 13 см -3 | 2000 | 1100 | 370 | 90 | 42 | — |
| SiC n-типа, концентрация атомов 10 17 см -3 , || оси c | 350 | 1900 | 5100 | 4100 | 1500 | 490 |
| PbS p-типа, n(при 27°С)=1,7·10 18 см -3 | 70 | 48 | 13 | 8,0 | — | — |
| PbS природный, n(при 27°С)=1,48·10 17 см -3 | — | — | — | 5,5 (-173°С) | 3,9 | 2,6 |
| PbSe p-типа, n(при 27°С)=5,4·10 18 см -3 | 70 | 37 | 11,5 | 5,2 | — | — |
| PbSe n-типа, n=6,4·10 17 см -3 , легированный медью | — | — | — | 5,0 | 3,0 | 1,8 |
| Bi2Te3 n-типа, n(при -196°С)=3·10 17 см -3 | — | — | — | 6,4 | 3,5 | 2,9 |
| AlN *3 | 65 | 100 | 175 | 290 | 330 | 200 |
| AlSb p-типа, R(при 27°С)=7,0 см 3 /Кл | 72 | 280 | 330 | 210 | 115 | 69 (-23°С) |
Примечание:
* 1 Приведены средние значения теплопроводимости ZnO гексагональной структуры: λср=1/3(2λа+λс), где λа и λс — теплопроводимости вдоль осей а и с соответственно. Для 30<Т<300 К λа/λс=1,2.
* 2 Горячепрессованная поликристаллическая керамика плотностью 97% теоретической, размер зернышек 20 мкм, концентрация примесей O и C меньше 2·10 19 см -3 .
* 3 Синтетический монокристалл, атомное содержание кислорода (1…5)·10 20 см -3 .
Обозначения: n — концентрация носителей тока; R — неизменная Хола.
- Охотин А.С., Боровикова Р.П. и др. Теплопроводимость жестких тел. Справочник. М.: Энергоатомиздат, 1984. — 320 с.
- Физические величины. Справочник. Под ред. И.С. Григорьева, Е.З. Мейлихова. М.: Энергоатомиздат, 1991. — 1232 с.
- Кайданов В.И., Нуромский А.Б. Электропроводность, термоэлектрические явления и теплопроводимость полупроводников. Учебное пособие. Ленинград, 1981. — 79 с.
- Стильбанс Л. С. Физика полупроводников. М.: Русское радио, 1967. — 451 с.
Характеристики оксидов металлов
Теплофизические характеристики оксидов металлов
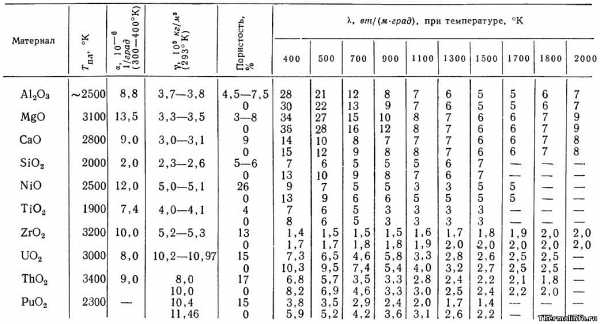
В таблице представлены теплофизические характеристики оксидов (спеченных окислов) металлов при различной температуре. Даны значения параметров последующих плотных спеченных окислов: оксиды алюминия и магния Al2O3, MgO, оксид кальция CaO, оксид кремния SiO2, оксид никеля NiO, оксид титана TiO, оксид циркония ZrO2, оксид урана UO2, оксид тория ThO2, оксид плутония PuO2
Теплопроводимость спеченных окислов в таблице указана при температуре от 127 до 1727 °С зависимо от пористости. Коэффициент линейного термического расширения (КТР) указан при температуре от 300 до 400 К. Плотность оксидов металлов дана при комнатной температуре.
Теплопроводимость спеченных оксидов металлов зависит от чистоты и кристаллической структуры начальных порошков, способа и степени прессования и режимов спекания. Теплопроводимость пылеобразных окислов зависит от плотности, размера зернышек и влажности; для всех пылеобразных оксидов металлов (не спеченных) теплопроводимость лежит в границах 0,1…1,1 Вт/(м·град).
В таблице даны последующие характеристики оксидов металлов:
- температура плавления, К;
- коэффициент линейного термического расширения (КТР), 1/град;
- плотность, кг/м 3 ;
- пористость, %;
- коэффициент теплопроводимости, Вт/(м·град).
Главные характеристики оксидов металлов
В таблице приведены главные характеристики оксидов металлов при комнатной температуре.
Характеристики указаны для последующих оксидов металлов: Al2O3, MgO, TiO, Ti2O3, TiO2, ZrO2, оксид цинка ZnO, оксиды железа FeO, Fe3O4, Fe2O3, NiO, оксид меди CuO, оксид ванадия V2O5, оксид вольфрама WO3, оксид марганца MnO2, оксид бария BaO2.
Какая плотность у сплава латуни

Латунь является двойным либо мультислойным сплавом на базе меди с главным легирующим элементом — цинком. Также нередко добавляют олово, железо, никель, свинец и марганец, остальные элементы. К бронзам по металлургической систематизации не относится.
Плотность материала — это физическая величина, которая описывает отношение массы материала к занимаемому размеру. Иными словами, плотностью именуют количество массы, находящейся в 1 единице размера. В системе СИ единицей измерения плотности принято считать кг/м 3 . Какова плотность латуни, можно выяснить из физических параметров сплава, величина плотности может изменяться зависимо от среды и критерий измерения. Плотность жестких веществ можно выяснить из справочной хим таблицы.
Латунь: плотность и характеристики

Латунь знакома людям еще с древности, по собственному наружному виду сплав припоминает золото, лишь стоит намного дешевле. Благодаря своим свойствам она сходу отыскала обширное применение, сплав был открыт в первый раз в Старом Риме, а потом повторно в 18 веке.
Наружный вид ее припоминает великодушный сплав, но в ней нет золота, базу составляет сплав цинка и меди и неких остальных частей, толика которых не наиболее 10%. Так как в составе меди много цинка и меди, то ее свойства весьма напоминают эти элементы. По собственному цвету, сплав может перебегать от желтых к красноватым колерам. Плотность составляет 8300-8700 кг/м 3 . Температура плавления латуни 880-950 о С, это зависит от ее состава, если содержится больше цинка, тогда температура плавления понижается. По собственной плотности латунь заходит в группу цветных металлов и сплавов.
При помощи контактной сварки латунь просто сваривается и отлично прокатывается. Если ее поверхность не покрыта лаком, она стремительно чернеет на воздухе, но в составе с иными сплавами она имеет большее сопротивление воздуху чем, к примеру, медь, весьма просто полируется.
Латунный сплав отлично поддается обработке в прохладном и жарком состоянии, имеет отличные механические свойства. По собственному наружному виду она весьма идентична с медью, но в отличие от меди латунь владеет высочайшей износоустойчивостью и прочностью. Латунь наименее тугоплавкая, но удобней в обработке, так как наиболее ковкая и вязкая.
От содержания в составе основного сплава будет зависеть тепло и электропроводность латуни, когда толика выше, тогда появляются сильней эти характеристики.
Значение латуни

Сплав меди с бронзой во все времена был весьма принципиальным для людей, но латунь также игралась свою важную роль в истории населения земли. Древнейшие римляне сплавляли цинк с рудой — галмеем, но таковой метод скоро устарел и в Великобритании сделали другое открытие, которое и захватило популярность.
Для получения латунного сплава использовались тигли, так температура могла достигнуть 1000 о С. Медь насыщалась парами цинка в итоге выходил готовый сплав, если не было остальных примесей. Дешевый и доступный метод получения латуни заполучил огромную популярность.
Температура плавления раздельно взятого цинка и меди очень различные, потому для облегчения получения готового сплава стала добавляться лигатура в незначимом количестве, но в готовом составе. В таком виде сплав упрощает задачку в промышленном производстве. Все латуни делятся на два вида:
- Двухкомпонентные — в составе цинка и меди с незначимым добавлением остальных примесей.
- Многокомпонентные — не считая обыкновенной меди и цинка находятся легирующие составляющие.
Применение латунного сплава
Относительно дешевый и легкий метод получения сплава его неповторимые характеристики дозволили стать ему всепригодным, потому сфер внедрения у него огромное количество. Из него вытягивают пруты и проволоку, штампуют в листы, также делают весьма узкую фольгу. Маленькие и большие детали, фурнитура, трубы, арматура употребляются в почти всех отраслях:
- Авто и хим индустрия
- Приборостроение
- Ювелирное дело
- В самолетостроении, разработке морских и речных судов
Цвет сплава весьма похож на золото, потому в ювелирном деле из него нередко делают декорации, он непревзойденно полируется. Когда за дело берется реальный мастер, то обыкновенному человеку трудно осознать, что это недрагоценный сплав. Бижутерия из латуни смотрится прекрасно и недешево.
В чистом виде медь весьма неустойчива к коррозии, а цинк является хрупким сплавом, при помощи сплава этих 2-ух видов сплава объединились их наилучшие характеристики и минимизировались недочеты.

- Деформированная разновидность — томпак, он характеризуется высочайшей прочностью, низкой силой трения и устойчивостью к ржавчине.
- Литейная — из нее делают фасонные изделия способом литья, также полуфабрикаты, Меди в ней содержится 50-81%. Этот вид не заржавевает, владеет высочайшими механическими качествами, комфортен в воззвании, благодаря водянистому состоянию, устойчив к трению с иными материалами.
- Автоматная латунь — благодаря собственной мягкости из нее делают пруты, листы, ленты и полосы.
- Ювелирные сплавы.
Заключение
В крайние годы спрос на латунный сплав лишь увеличивается в главном она пользуется спросом на азиатском рынке. Его также приобретают и развитые экономические страны, к примеру, европейские, США (Соединённые Штаты Америки — государство в Северной Америке) . Уровень производства латуни зависит от ее спроса, также от мирового рынка меди.
 Цинк — хрупкий переходный сплав голубовато-белого цвета (тускнеет на воздухе, покрываясь узким слоем оксида цинка). Эссенциальный (неподменный) микроэлемент тканей человека. По количественному соотношению в организме занимает 2-ое, опосля железа, пространство. Ему принадлежит главная роль в регенерации покоробленных тканей, потому что без цинка нарушается синтез нуклеиновых кислот и белка.
Цинк — хрупкий переходный сплав голубовато-белого цвета (тускнеет на воздухе, покрываясь узким слоем оксида цинка). Эссенциальный (неподменный) микроэлемент тканей человека. По количественному соотношению в организме занимает 2-ое, опосля железа, пространство. Ему принадлежит главная роль в регенерации покоробленных тканей, потому что без цинка нарушается синтез нуклеиновых кислот и белка.
Смотрите так же:
СТРУКТУРА
СВОЙСТВА
 При комнатной температуре хрупок, при сгибании пластинки слышен треск от трения кристаллитов (обычно посильнее, чем «вопль олова»). Имеет низкую температуру плавления. Размер сплава при плавлении возрастает в согласовании со понижением плотности. С увеличением температуры миниатюризируется кинетическая вязкость и электропроводность цинка и увеличивается его удельное электронное сопротивление. При 100—150 °C цинк пластичен. Примеси, даже незначимые, резко наращивают хрупкость цинка. Является диамагнетиком.
При комнатной температуре хрупок, при сгибании пластинки слышен треск от трения кристаллитов (обычно посильнее, чем «вопль олова»). Имеет низкую температуру плавления. Размер сплава при плавлении возрастает в согласовании со понижением плотности. С увеличением температуры миниатюризируется кинетическая вязкость и электропроводность цинка и увеличивается его удельное электронное сопротивление. При 100—150 °C цинк пластичен. Примеси, даже незначимые, резко наращивают хрупкость цинка. Является диамагнетиком.
ЗАПАСЫ И ДОБЫЧА
 Среднее содержание цинка в земной коре — 8,3·10 -3 %, в главных извержённых породах его несколько больше (1,3·10 -2 %), чем в кислых (6·10 -3 %). Цинк — энергичный аква мигрант, в особенности свойственна его миграция в термальных водах вкупе со свинцом. Из этих вод осаждаются сульфиды цинка, имеющие принципиальное промышленное значение. Цинк также энергично мигрирует в поверхностных и подземных водах, основным осадителем для него является сероводород, наименьшую роль играет сорбция глинами и остальные процессы.
Среднее содержание цинка в земной коре — 8,3·10 -3 %, в главных извержённых породах его несколько больше (1,3·10 -2 %), чем в кислых (6·10 -3 %). Цинк — энергичный аква мигрант, в особенности свойственна его миграция в термальных водах вкупе со свинцом. Из этих вод осаждаются сульфиды цинка, имеющие принципиальное промышленное значение. Цинк также энергично мигрирует в поверхностных и подземных водах, основным осадителем для него является сероводород, наименьшую роль играет сорбция глинами и остальные процессы.
Месторождения цинка известны в Иране, Австралии, Боливии, Казахстане. В Рф наикрупнейшим производителем свинцово-цинковых концентратов является ОАО (форма организации публичной компании; акционерное общество) «ГМК Дальполиметалл»
Цинк добывают из полиметаллических руд, содержащих 1—4% Zn в виде сульфида, также Cu, Pb, Ag, Au, Cd, Bi. Руды обогащают селективной флотацией, получая цинковые концентраты (50—60% Zn) и сразу свинцовые, медные, а время от времени также пиритные концентраты.
Главный метод получения цинка — электролитический (гидрометаллургический). Обожжённые концентраты обрабатывают серной кислотой; получаемый сульфатный раствор очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу в ваннах, плотно выложенных снутри свинцом либо винипластом. Цинк осаждается на дюралевых катодах, с которых его ежесуточно убирают (сдирают) и плавят в индукционных печах.
ПРОИСХОЖДЕНИЕ
 Цинк в природе как самородный сплав не встречается. Понятно 66 минералов цинка, а именно цинкит, сфалерит, виллемит, каламин, смитсонит, франклинит. Более всераспространенный минерал — сфалерит, либо цинковая обманка. Главный компонент минерала — сульфид цинка ZnS, а различные примеси присваивают этому веществу различные цвета. Из-за трудности определения этого минерала его именуют обманкой (др.-греч. σφαλερός — обманчивый). Цинковую обманку считают первичным минералом, из которого образовались остальные минералы элемента № 30: смитсонит ZnCO3, цинкит ZnO, каламин 2ZnO · SiO2 · Н2O. На Алтае часто можно повстречать полосатую «бурундучную» руду — смесь цинковой обманки и бурого шпата. Кусочек таковой руды издалече вправду похож на затаившегося полосатого зверя.
Цинк в природе как самородный сплав не встречается. Понятно 66 минералов цинка, а именно цинкит, сфалерит, виллемит, каламин, смитсонит, франклинит. Более всераспространенный минерал — сфалерит, либо цинковая обманка. Главный компонент минерала — сульфид цинка ZnS, а различные примеси присваивают этому веществу различные цвета. Из-за трудности определения этого минерала его именуют обманкой (др.-греч. σφαλερός — обманчивый). Цинковую обманку считают первичным минералом, из которого образовались остальные минералы элемента № 30: смитсонит ZnCO3, цинкит ZnO, каламин 2ZnO · SiO2 · Н2O. На Алтае часто можно повстречать полосатую «бурундучную» руду — смесь цинковой обманки и бурого шпата. Кусочек таковой руды издалече вправду похож на затаившегося полосатого зверя.
ПРИМЕНЕНИЕ
 Незапятнанный железный цинк употребляется для восстановления великодушных металлов, добываемых подземным выщелачиванием (золото, серебро). Не считая того, цинк употребляется для извлечения серебра, золота (и остальных металлов) из предварительного свинца в виде интерметаллидов цинка с серебром и золотом (так именуемой «серебристой пены»), обрабатываемых потом обыкновенными способами аффинажа.
Незапятнанный железный цинк употребляется для восстановления великодушных металлов, добываемых подземным выщелачиванием (золото, серебро). Не считая того, цинк употребляется для извлечения серебра, золота (и остальных металлов) из предварительного свинца в виде интерметаллидов цинка с серебром и золотом (так именуемой «серебристой пены»), обрабатываемых потом обыкновенными способами аффинажа.
Применяется для защиты стали от коррозии (оцинковка поверхностей, не подверженных механическим действиям, либо металлизация — для мостов, емкостей, металлоконструкций).
Цинк употребляется в качестве материала для отрицательного электрода в хим источниках тока, другими словами в батарейках и аккумах.
Пластинки цинка обширно употребляются в полиграфии, а именно, для печати иллюстраций в многотиражных изданиях. Для этого с XIX века применяется цинкография — изготовка клише на цинковой пластинке с помощью вытравливания кислотой рисунка в ней. Примеси, кроме маленького количества свинца, усугубляют процесс травления. Перед травлением цинковую пластинку подвергают отжигу и прокатывают в нагретом состоянии.
Цинк вводится в состав почти всех твёрдых припоев для понижения их температуры плавления.
Окись цинка обширно употребляется в медицине как антисептическое и антивосполительное средство. Также окись цинка употребляется для производства краски — цинковых белил.
Цинк — принципиальный компонент латуни. Сплавы цинка с алюминием и магнием (ЦАМ, ZAMAK) благодаря сравнимо высочайшим механическим и весьма высочайшим литейным качествам весьма обширно употребляются в машиностроении для четкого литья. А именно, в оружейном деле из сплава ZAMAK (-3, −5) время от времени отливают затворы пистолетов, в особенности рассчитанных на внедрение слабеньких либо травматических патронов. Также из цинковых сплавов отливают различную техно фурнитуру, вроде авто ручек, корпусы карбюраторов, масштабные модели и различные миниатюры, также любые остальные изделия, требующие четкого литья при применимой прочности.
Хлорид цинка — принципиальный флюс для пайки металлов и компонент при производстве фибры.
Теллурид, селенид, фосфид, сульфид цинка — обширно используемые полупроводники. Сульфид цинка — составная часть почти всех люминофоров. Фосфид цинка употребляется в качестве отравы для грызунов.
Селенид цинка употребляется для производства оптических стёкол с весьма низким коэффициентом поглощения в среднем инфракрасном спектре, к примеру, в углекислотных лазерах.
- 5 – 9 классы
- Химия
- 5 баллов
тепло-и электропроводность : МЕДИ. ЖЕЛЕЗА. МАГНИЯ . ЦИНКА. АЛЮМИНИЯ . НАТРИЯ .
СРОЧНООООООООООООООООООООО
- Попроси больше разъяснений
- Смотреть
- Отметить нарушение
Ответ
Медь-тепл.382—390Вт/(м·К) электро58 100 000 см/м
железо-тепл.92Вт/(м·К) электро10 000 000 см/м
магний-тепл.156 Вт/(м·К) электро 22 700 000
Цинк-тепл.116 Вт/(м·К) электро16 900 000
алюминий-тепл.237 Вт/(м·К)электро(37·106 См/м)
Цинк – Сплав, Придающий МУЖСКУЮ СИЛУ! (Aug 2019).
Цинк (Zn) – это обильный сплав, обнаруженный в земной коре с обилием промышленных и био применений.
При комнатной температуре цинк является хрупким и сине-белым цветом, но быть может отполирован до броского конца.
Главный сплав, цинк сначала употребляется для гальванизации стали, для защиты сплава от ненужной коррозии. Но сплавы цинка, в том числе латунные, актуально важны для широкого диапазона применений: от коррозионно-стойких морских компонент до музыкальных инструментов.
Физические характеристики
- Сила: Цинк – слабенький сплав с прочностью на разрыв наименее половины, чем у мягенькой углеродистой стали. Обычно, он не употребляется в несущих отягощениях, хотя дешевые механические детали могут быть отлиты из цинка.
- Твердость: Незапятнанный цинк имеет низкую вязкость и обычно хрупкий, но цинковые сплавы обычно имеют высшую ударную вязкость по сопоставлению с иными литейными сплавами.
- Пластичность: Меж 212-302 o F цинк становится пластичным и ковким, но при завышенных температурах ворачивается в хрупкое состояние. Снова же, сплавы цинка существенно делают лучше это свойство по сопоставлению с незапятнанным сплавом, что дозволяет применять наиболее сложные способы производства.
- Электропроводность: Проводимость цинка умеренная для сплава. Но его мощные химические характеристики отлично работают в процессе гальванизации и щелочных батарей
История
Изделия из цинкового сплава, сделанные человеком, были накрепко датированы еще в 500 г. до н.э., а цинк был за ранее преднамеренно добавлен к меди с образованием латуни около 200-300 г. до н.э.
Латунь дополняла бронзу во время Римской империи при изготовлении монет, орудия и искусства и оставалась основным внедрением цинка до 1746 года, когда Андреас Сигизмунд Маргграф сознательно изолировал незапятнанный элемент. Так как он кропотливо описывал собственный процесс и как он работал, цинк скоро был коммерчески доступен.
Алессандро Вольта сделал первую батарею в 1800 году с внедрением медных и цинковых пластинок, введя новейшую эру электронных познаний. К 1837 году Станислав Сорель именовал собственный новейший процесс цинкования, гальванизации, опосля Луиджи Гальвани, который нашел оживляющий эффект электро энергии при аутопсии лягушек. Гальванизация, форма катодной защиты, может защитить огромное количество металлов и в истинное время является главным фабричным применением незапятнанного цинка.
Цинк в торговой зоне
Цинк в главном извлекается из руды, содержащей сульфид цинка, цинковая обманка либо сфалерит.
Страны, добывающие и выпускающие самый неповторимый цинк в порядке убывания, – это Китай, Перу, Австралия, США (Соединённые Штаты Америки — государство в Северной Америке) и Канада. Согласно геологической службе США (Соединённые Штаты Америки — государство в Северной Америке), в 2014 году было добыто около 13,4 млн. Тонн цинка в концентрате, на долю Китая приходится около 36 процентов от общего размера.
По данным Интернациональной исследовательской группы свинца и цинка, в 2013 году в гальванических, латунных и бронзовых сплавах, цинковых сплавах, хим производстве и литье под давлением было израсходовано около 13 миллионов метрических тонн цинка.
Цинк торгуется на LME как договоры «Special High Grade» при 99. 995% малой чистоте в 25-тонных слитках.






























